üĒį┤Ż║ŠWĮj┘Yį┤ 2022-11-24 16:31:42
╬’┘|ų«ķgĄ─▐DōQų„ę¬┐╝▓ķ╗»īWĘĮ│╠╩ĮŻ¼╬’┘|Ą─═ŲöÓĖ³ŠC║Ž┐╝▓ķ╬’┘|Ą─├¹ĘQŻ¼╦ūĘQĪóė├═ŠŻ¼│Ż┐╝Ą─╗»īWĘĮ│╠╩Į╝░¼FŽ¾Ż¼│ŻęŖ╬’┘|ų«ķgĄ─▐DōQę╗ȩ꬚Ų╬šĄ─ĘŪ│Ż└╬╣╠ĪŻ┐╝Ņ}į┌├┐▒ŠĮ╠▌o╔Ž├µČ╝ėąŻ¼▓╗į┘┴_┴ąŻ¼║åå╬░čš¹└ĒĄ─ų¬ūR³cš╣¼F│÷üĒĪŻ
│ŻęŖ╬’┘|ķgĄ─╚²ĮŪ▐DōQłDŻ║
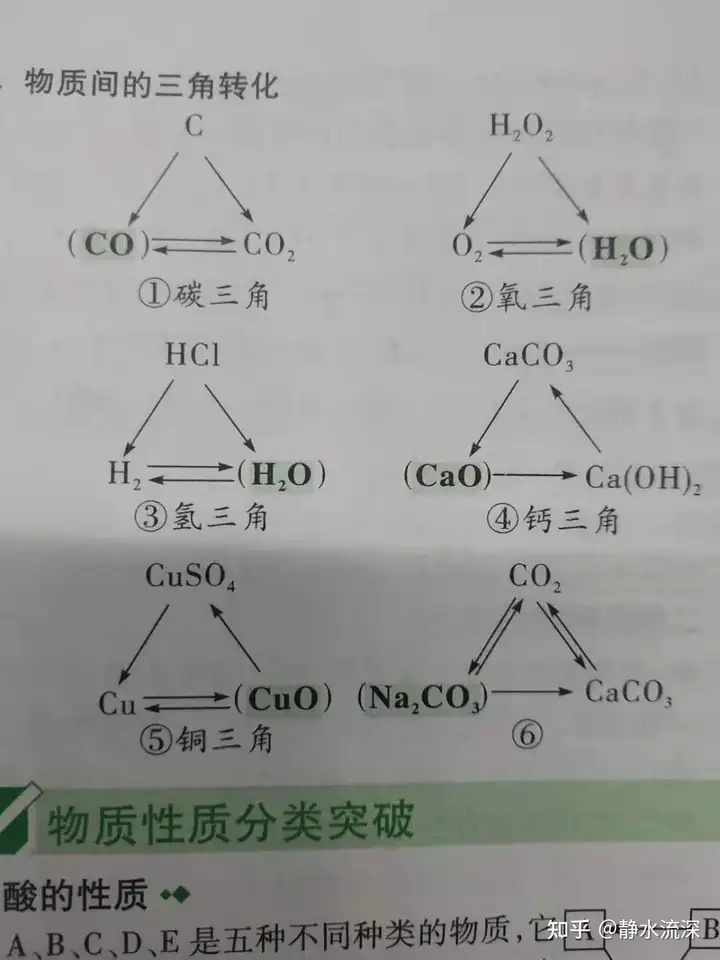
▀@ą®╔µ╝░Ą─╗»īWĘĮ│╠╩Įę╗Č©ę¬ĘŪ│ŻĄ─╩ņŽżĪŻę▓┐╔ęį▀@śė╚ź▀Mę╗▓Įš¹└ĒŻ¼╚ńłDŻ║
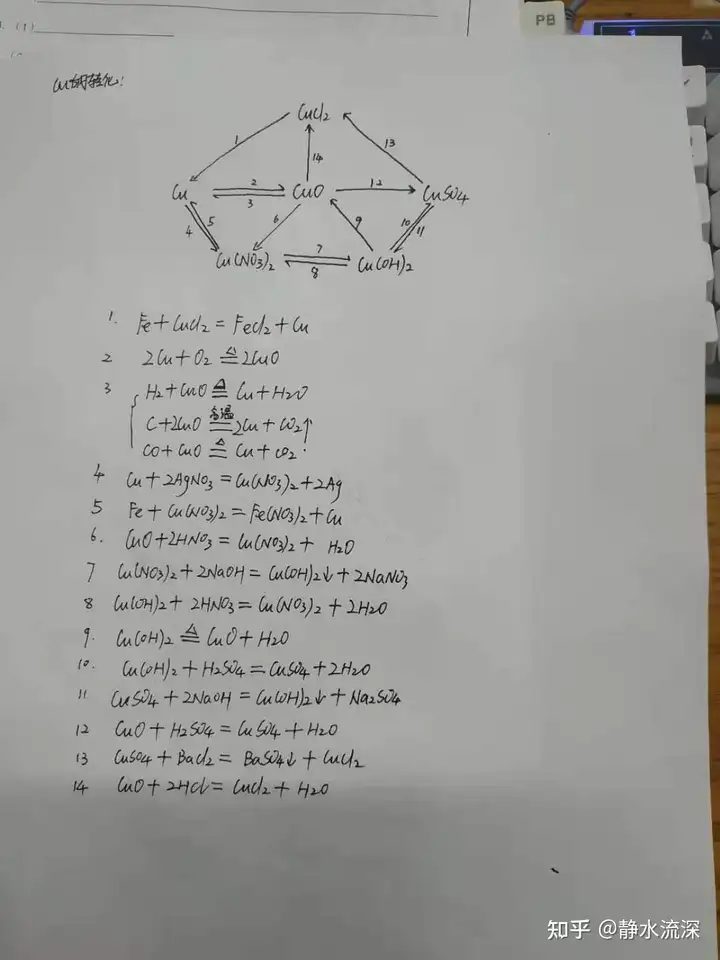
═©▀^ė^▓ņŻ¼┐╔ęį░l¼F▀@ą®▐DōQĻPŽĄłD╔µ╝░Ą─╗»īWĘĮ│╠╩ĮŠ═Ģ■ėąųžÅ═Ą─Ż¼Įø│ŻųžÅ═Ą─┐ŽČ©╩Ū▒ž┐╝Ą─Ż¼ę╗Č©ę¬└╬ėøĪŻ
«ö╚╗═ŲöÓŅ}ųąŻ¼▀Ćę¬ę└ō■Ņ}ęŌŻ¼║åå╬╚ź┼ąöÓ╬’┘|╩Ū╩▓├┤Ż¼Ė∙ō■Ņ}ęŌ┤¾Ė┼▓┬£y│÷üĒ╩Ū╩▓├┤└²ūėŻ¼╩▓├┤ŅÉą═Ą─╬’┘|Ż¼╚╗║¾į┘ī”æ¬╚źÄ¦╚ļŻ¼╦╝┐╝╗»īWĘĮ│╠╩Į╩ŪĘ±Ę¹║ŽŅ}ęŌĪŻ▒╚╚ńŻ¼Ņ}Ė╔šf“▓╗═¼ŅÉäeĄ─╬’┘|”Ż¼╝┤ųĖ▀@ą®╬’┘|╩Ū╦ßĪóēAĪó¹}Īóč§╗»╬’Īóå╬┘|ųąĄ──│ĘNĄ╚Ą╚ĪŻ║åå╬╬’┘|Ą─└Ē╗»ąį┘|┐éĮY╚ńŽ┬Ż║
│ŻęŖ╬’┘|Ą─├¹ĘQĪó╗»īWĪó╦ūĘQĪóė├═Š
1.┬╚╗»Ōc(NaCl)Ż║╩│¹};ū÷š{╬Č䮯¼▒∙讎¹╚┌䮯¼ßtė├╔·└Ē¹}╦«;▐rśI╔Ž▀xĘNĪŻ
2.╠╝╦ßŌc(Na2CO3)Ż║╝āēAŻ¼╠K┤“Ż¼╩Ū¹}▓╗╩ŪēAŻ¼╚▄ė┌╦«│╩ēAąįŻ¼─▄╩╣Ęė╠¬ūā╝t;ė├ė┌▓Ż┴¦╗»╣ż╣żśIŻ¼Ę╩įĒŻ¼╝Å┐ŚĪŻ
3.Üõč§╗»Ōc(NaOH)Ż║╗ēAŻ¼¤²ēAŻ¼┐┴ąįŌc;ĀtŠ▀ŪÕØŹä®Ą─ų„ę¬│╔Ęų;╣╠¾węū│▒ĮŌŻ¼╚▄ė┌╦«Ę┼¤ß;┐╔ū÷Ė╔į’ä®(▓╗─▄Ė╔į’CO2);┐╔ū÷╗»╣żįŁ┴ŽŻ¼ė├ė┌Ę╩įĒŻ¼╩»ė═Ż¼įņ╝ł;╔·╗Ņųą│²ė═╬█ĪŻ
4.č§╗»Ō}(CaO)Ż║╔·╩»╗ę;ū÷Ė╔į’䮯¼║═╦«Ę┤æ¬Ę┼¤ß;CaO + H2O = Ca(OH)2 .
5.Üõč§╗»Ō}(Ca(OH)2)Ż║╩ņ╩»╗ęŻ¼Ž¹╩»╗ęŻ¼╩»╗ę╚ķĄ─ų„ę¬│╔Ęų;īŹ“×╩ęÖz“×CO2;ė├ė┌Į©ų■▓─┴Ž;▐rśI╔Ž║═CuSO4┼õų├▐r╦Ä▓©Ā¢ČÓę║;Ė─┴╝╦ßąį═┴╚└ĪŻ
6.Č■č§╗»╠╝╣╠¾w(CO2)Ż║Ė╔▒∙;įņ│╔£ž╩깦æ¬;ū÷ÜŌ¾wĘ╩┴Ž;£ń╗;╚╦╣żĮĄėĻ;╬Ķ┼_įņņFä®ĪŻ
7.Üõ┬╚╦ß(HCl)Ż║¹}╦ß;╬Ė╦ߥ─ų„ę¬│╔Ęų;┐╔ū÷│²õPä®;
8.ēA╩Į╠╝╦ßŃ~(Cu2(OH)2CO3)Ż║Ń~ŠGŻ¼┐ū╚Ė╩»Ą─ų„ę¬│╔ĘųĪŻ
9.┴“╦ßŃ~Š¦¾w(CuSO4•5H2O)Ż║╦{Ą\Ż¼─æĄ\ĪŻ
10.╝ū═ķ(CH4)Ż║šėÜŌŻ¼═▀╦╣ÜŌŻ¼┐ėÜŌŻ¼╠ņ╚╗ÜŌŻ¼┐╔╚╝▒∙Ą─ų„ę¬│╔Ęų;ūŅ║åå╬ėąÖC╬’Ż¼ŪÕØŹ─▄į┤Ż¼ę▓╩Ūįņ│╔£ž╩ęą¦æ¬Ą─ÜŌ¾wų«ę╗ĪŻ
11.ęę┤╝(C2H5OH)Ż║ŠŲŠ½Ż¼ŪÕØŹ─▄į┤Ż¼┐╔į┘╔·┘Yį┤ĪŻ
12.ęę╦ß(CH3COOH)Ż║┤ū╦߯¼ÅNĘ┐š{╬ČŲĘ;┐╔ė├ė┌│²╦«╣Ė;
13.▀^č§╗»Üõ(H2O2)Ż║ļpč§╦«
14.╣»(Hg)Ż║╦«ŃyŻ¼│Ż£žŽ┬╬©ę╗│╩ę║æBĄ─Įī┘ĪŻ
15.╠╝╦ßÜõŌc(NaHCO3)Ż║ąĪ╠K┤“;ų╬»¤╬Ė╦ß▀^ČÓ;░lĮ═Ę█Ą─ų„ę¬│╔Ęų;ė├ė┌▒║ųŲĖŌ³cĪŻ
16.č§ÜŌO2Ż║ę║æB│╩╦{╔½Ż¼ė├ė┌¤ÆõōŻ¼ßt»¤╝▒Š╚Ż¼╣®Įo║¶╬³;ėąų·╚╝ąįŻ¼č§╗»ąįĪŻ
17.ÜõÜŌH2Ż║├▄Č╚ūŅąĪĄ─ÜŌ¾w;ūŅŪÕØŹ─▄į┤;ā׳cŻ║¤ßųĄĖ▀Ż¼įŁ┴ŽüĒį┤ÅV;«a╬’¤o╬█╚Š;
18.╠╝╦ßŌ}CaCO3Ż║┤¾└Ē╩»Īó╩»╗ę╩»Ą─ų„ę¬│╔Ęų;ė├ė┌ū÷Į©ų■▓─┴ŽŻ¼čaŌ}ä®ĪŻ
19.CuSO4;░ū╔½╣╠¾wŻ¼ė÷╦«ūā╦{Ż¼┐╔Ķbäe╩Ūʱėą╦«Ą─┤µį┌;┐╔┼õų├▐r╦Ä▓©Ā¢ČÓę║ĪŻ
20.ØŌ┴“╦߯║ėą╬³╦«ąįŻ¼┐╔ū÷Ė╔į’䮯¼Ą½▓╗─▄Ė╔į’NH3;ķLŲ┌ų├ė┌┐šÜŌųąĢ■╬³╩š┐šÜŌųąĄ─╦«š¶ÜŌČ°╚▄ę║Ą─┘|┴┐į÷╝ėŻ¼ØŌČ╚Ģ■Ž┬ĮĄĪŻŽĪ┴“╦ß┐╔ū÷│²õPä®ĪŻ
21.ØŌ¹}╦߯║ėąō]░ląįĪŻ┤“ķ_Ų┐╚¹Ų┐┐┌│÷¼F░ūņF;ķLŲ┌ų├ė┌┐šÜŌųąŻ¼╚▄┘|(HCl)ō]░lČ°╚▄┘|Ą─┘|┴┐ĘųöĄŽ┬ĮĄĪŻ
22.╠╝╦ßŌøK2CO3Ż║▓▌─Š╗ęĄ─ų„ę¬│╔ĘųŻ¼╚▄ė┌╦«│╩ēAąįŻ¼▓╗─▄║═õ@æBĄ¬Ę╩╗ņė├ĪŻ
http://23.COŻ║ėąČŠÜŌ¾wŻ¼¤o╔½¤o╬Č;║═č¬╝tĄ░░ūĮY║Žįņ│╔ę╗č§╗»╠╝ųąČŠ;┐╔╚╝ąį║═▀ĆįŁąį┐╔ū÷╚╝┴Ž║═ė├ė┌Įī┘Ą─ę▒¤ÆĪŻ
24.N2Ż║ū÷▒ŻūoÜŌĪŻ╩│ŲĘ░³čb┤³ā╚Ą─│õĄ─ÜŌ¾węįĘ└Ė»;ė├ė┌╗»Ę╩Ż¼Ž§╦ߥ─ųŲ╚ĪĪŻ
25.ŽĪėąÜŌ¾wŻ║ČĶąįÜŌ¾wŻ¼╗»īWąį┘|ĘĆČ©;ė├ė┌─▐║ń¤¶Ż¼╠Ņ│õ╠Į┐šÜŌŪ“Ą─ÜŌ¾w(║żÜŌHe)║═║ĖĮėĮī┘Ą─▒ŻūoÜŌĪŻ
26.╠╝C Ż║┐╔╚╝ąįū÷╚╝┴Ž;▀ĆįŁąįė├ė┌ę▒¤ÆĮī┘Ż¼║═CO2Ė▀£ž╔·│╔CO;│Ż£žŽ┬╣┼┤·ūų«ŗė├Ą─╠╝╦ž─½ųŁšf├„╠╝Ą─ĘĆČ©ąįĪŻ
ėąĢr║“▀Ćėąę╗ą®ą┼Žó┐╔ęį═Ų£y╩Ū─│ą®╬’┘|Ż¼▒╚╚ń│ŻęŖĄ─╬’┘|į┌╚▄ę║ųąĄ─Ņü╔½Ż¼╬’┘|─│ĘNį¬╦žĄ─ŽÓī”Ęųūė┘|┴┐Ą╚ĪŻ║åå╬ū÷╚ńŽ┬┐éĮYŻ║
│ŻęŖ╬’┘|Ą─Ņü╔½
╣╠¾wĄ─Ņü╔½
1.╝t╔½╣╠¾wŻ║Ń~Ż¼č§╗»ĶFŻ¼č§╗»╣»
2.ŠG╔½╣╠¾wŻ║ēA╩Į╠╝╦ßŃ~(Ń~ŠG)
3.╦{╔½╣╠¾wŻ║Üõč§╗»Ń~Ż¼┴“╦ßŃ~Š¦¾w
4.ūŽ║┌╔½╣╠¾wŻ║Ė▀Õi╦ßŌø
5.ĄŁ³S╔½╣╠¾wŻ║┴“╗Ū
6.¤o╔½╣╠¾wŻ║▒∙Ż¼Ė╔▒∙Ż¼Įäé╩»
7.Ńy░ū╔½╣╠¾wŻ║ŃyŻ¼ĶFŻ¼µVŻ¼õXŻ¼Ą╚Įī┘
8.║┌╔½╣╠¾wŻ║ĶFĘ█Ż¼─Š╠┐Ż¼č§╗»Ń~Ż¼Č■č§╗»ÕiŻ¼╦─č§╗»╚²ĶFŻ¼(╠╝║┌Ż¼╗Ņąį╠┐)
9.╝t║ų╔½╣╠¾wŻ║Üõč§╗»ĶF
10.░ū╔½╣╠¾wŻ║┬╚╗»ŌcŻ¼╠╝╦ßŌcŻ¼Üõč§╗»ŌcŻ¼Üõč§╗»Ō}Ż¼╠╝╦ßŌ}Ż¼č§╗»Ō}Ż¼┴“╦ßŃ~Ż¼╬Õč§╗»Č■┴ūŻ¼č§╗»µV
ę║¾wĄ─Ņü╔½
1.Ę▓║¼Cu2+Ą─╚▄ę║│╩╦{╔½;┴“╦ßŃ~╚▄ę║Ż¼┬╚╗»Ń~╚▄ę║Ż¼Ž§╦ßŃ~╚▄ę║;
2.Ę▓║¼Fe2+Ą─╚▄ę║│╩£\ŠG╔½Ż║┴“╦ßüåĶF╚▄ę║Ż¼┬╚╗»üåĶF╚▄ę║Ż¼Ž§╦ßüåĶF╚▄ę║;
3.Ę▓║¼Fe3+Ą─╚▄ę║│╩ūž³S╔½Ż║┴“╦ßĶF╚▄ę║Ż¼┬╚╗»ĶF╚▄ę║Ż¼Ž§╦ßĶF╚▄ę║;
4.¤o╔½ę║¾wŻ║╦«Ż¼ļpč§╦«;
5.ūŽ╝t╔½╚▄ę║Ż║Ė▀Õi╦ßŌø╚▄ę║;
6.ūŽ╔½╚▄ę║Ż║╩»╚’╚▄ę║ ŲõėÓ╚▄ę║ę╗░ŃŠ∙×ķ¤o╔½;
į┘ĖĮę╗Ę▌Ż║
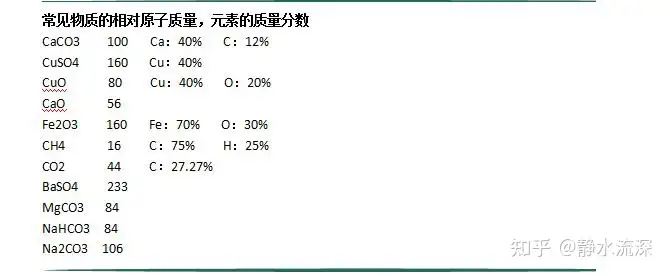
«ö╚╗Ż¼▀Ćėą║▄ČÓ┴Ń╦ķĄ─ų¬ūR³cŻ¼▀@éĆ┤¾╝ę┐╔ęį└^└mča│õŻ¼▒╚╚ń─┐Ū░ė├┴┐ūŅ┤¾Ą─Įī┘╩ŪĶFĄ╚Ą╚Ż¼ę╗Č©ČÓÜw╝{ČÓ┐éĮYĪŻ
ĪĪĪĪ ÜgėŁ╩╣ė├╩ųÖCĪóŲĮ░ÕĄ╚ęŲäėįOéõįLå¢ųą┐╝ŠWŻ¼2025ųą┐╝ę╗┬Ę┼Ń░ķ═¼ąąŻĪ>>³cō¶▓ķ┐┤